
Health Education , Health Promotion and Educational Technology
آموزش بهداشت ، ارتقا سلامت و تکنولوژی آموزشی
Health Education , Health Promotion and Educational Technology
آموزش بهداشت ، ارتقا سلامت و تکنولوژی آموزشیچاقی و اضافه وزن پیش رونده اما متفاوت
گزارش سازمان جهانی بهداشت (WHO)
2024.03.01

حقایق کلیدی
- در سال 2022، از هر 8 نفر در جهان یک نفر با چاقی زندگی می کرد.
- چاقی بزرگسالان در سراسر جهان از سال 1990 بیش از دو برابر شده است و چاقی نوجوانان چهار برابر شده است.
- در سال 2022، 2.5 میلیارد بزرگسال (18 سال و بالاتر) اضافه وزن داشتند. از این تعداد، 890 میلیون نفر با چاقی زندگی می کردند.
- در سال 2022، 43 درصد از بزرگسالان 18 سال و بالاتر دارای اضافه وزن و 16 درصد مبتلا به چاقی بودند.
- در سال 2022، 37 میلیون کودک زیر 5 سال دارای اضافه وزن بودند.
- بیش از 390 میلیون کودک و نوجوان 5 تا 19 ساله در سال 2022 دارای اضافه وزن بودند، از جمله 160 میلیون نفر که با چاقی زندگی می کردند.
اضافه وزن و چاقی

اضافه وزن وضعیتی است که در آن تجمع بیش از حد چربی وجود دارد.
چاقی یک بیماری پیچیده مزمن است که با رسوبات بیش از حد چربی تعریف می شود که می تواند سلامت را مختل کند. چاقی می تواند منجر به افزایش خطر ابتلا به دیابت نوع 2 و بیماری قلبی شود، می تواند بر سلامت استخوان وقدرت باروری تأثیر بگذارد، خطر ابتلا به برخی سرطان ها را افزایش می دهد. چاقی بر کیفیت زندگی مانند خواب یا حرکت تأثیر می گذارد.
تشخیص اضافه وزن و چاقی با اندازه گیری وزن و قد افراد و با محاسبه شاخص توده بدنی (BMI)(Body Mass Index): وزن (kg) / قد مترمربع (m²) انجام می شود(یعنی وزن برحسب کیلوگرم تقسیم بر قد بر حسب متر به توان دو). شاخص توده بدنی نشانگر جایگزینی برای چاقی است و اندازه گیری های اضافی مانند دور کمر می تواند به تشخیص چاقی کمک کند. دقت داشته باشید دسته بندی BMI برای تعریف چاقی بر اساس سن و جنسیت در نوزادان، کودکان و نوجوانان متفاوت از بزرگسالان (یعنی افراد بالای 18 سال) است.
تعریف WHO برای اضافه وزن و چاقی در بزرگسالان
در بزرگسالان (افراد بالای 18 سال )
BMI بزرگتر یا مساوی 25 تا 29.9باشد یعنی فرد اضافه وزن (Over weight) دارد و اگر
BMI بزرگتر یا مساوی 30 باشد یعنی فرد دچار بیماری چاقی (Obesity) هست.
برای کودکان، سن باید در تعریف اضافه وزن و چاقی در نظر گرفته شود.
در کودکان زیر 5 سال
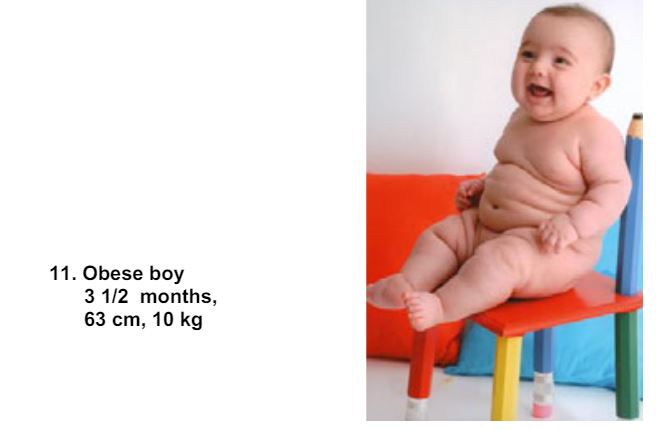
(تصویر : یک پسر چاق، سه ماه نیم، وزن 10 کیلوگرم، قد 63 سانتی متر)
اضافه وزن: وزن به قد بیشتر از 2 انحراف معیار بالاتر از میانگین استانداردهای رشد کودکان در سازمان جهانی بهداشت است.
چاقی : وزن به قد بیش از 3 انحراف معیار بالاتر از میانگین استانداردهای رشد کودکان سازمان جهانی بهداشت است.
نمودارها و جداول: استانداردهای رشد کودک سازمان جهانی بهداشت برای کودکان زیر 5 سال اینجا ببینید.
https://www.who.int/tools/child-growth-standards
در افراد بین 5 تا 19 سال

اضافه وزن: BMI به سن بیشتر از 1 انحراف معیار بالاتر از میانه مرجع رشد WHO است.
چاقی: BMI به سن بیش از 2 انحراف معیار بالاتر از میانه مرجع رشد WHO است.
نمودارها و جداول: مرجع رشد سازمان بهداشت جهانی برای افراد 5 تا 19 ساله را اینجا ببینید.
https://www.who.int/tools/growth-reference-data-for-5to19-years
در حالی که تنها 2 درصد از کودکان و نوجوانان 5 تا 19 ساله در سال 1990 چاق بودند (31 میلیون )، تا سال 2022، 8 درصد از کودکان و نوجوانان با چاقی زندگی می کردند (160 میلیون جوان).
علل اضافه وزن و چاقی
اضافه وزن و چاقی ناشی از عدم تعادل انرژی دریافتی (رژیم غذایی) و مصرف انرژی (فعالیت بدنی) است.
در اغلب موارد چاقی یک بیماری چند عاملی است که به دلیل محیط های چاق کننده، عوامل روانی- اجتماعی و ژنتیکی ایجاد می شود. در یک زیرگروه از بیماران، عوامل اصلی منفرد را می توان در ایجاد چاقی شناسایی کرد که مواردی نظیر برخی ازداروها، بیماری ها، بی حرکتی، روش های ایتروژنیک، بیماری تک ژنی / سندرم ژنتیکی می باشد.
محیط چاق کننده که احتمال چاقی را در افراد، جمعیتها و در محیطهای مختلف تشدید میکند، به عوامل ساختاری محدودکننده دسترسی به غذای سالم پایدار با قیمتهای مقرونبهصرفه محلی، عدم تحرک فیزیکی ایمن و آسان در زندگی روزمره همه افراد و عدم وجود آن محیط قانونی و نظارتی کافی مرتبط است.
در عین حال، فقدان یک پاسخ موثر سیستم بهداشتی برای شناسایی افزایش وزن اضافی و رسوب چربی در مراحل اولیه، پیشرفت به سمت چاقی را تشدید می کند.
خطرات سلامتی ناشی از اضافه وزن و چاقی
در سال 2019، BMI بالاتر از حد مطلوب (یعنی BMI مساوی یا بیشتر از 25) باعث مرگ 5 میلیون نفر در اثر بیماری های غیرواگیر (NCDs) مانند بیماری های قلبی عروقی، دیابت، سرطان ها، اختلالات عصبی، بیماری های مزمن تنفسی و اختلالات گوارشی شد.
اضافه وزن در دوران کودکی و نوجوانی بر آینده سلامت کودکان و نوجوانان تأثیر می گذارد و با خطر بیشتر و شروع زودتر بیماری های غیرواگیر مختلف مانند دیابت نوع 2 و بیماری های قلبی عروقی مرتبط است. چاقی دوران کودکی و نوجوانی پیامدهای روانی - اجتماعی نامطلوبی دارد. عملکرد مدرسه و کیفیت زندگی را تحت تأثیر قرار می دهد که با انگ، تبعیض و قلدری ترکیب می شود. کودکان چاق به احتمال زیاد بزرگسالان مبتلا به چاقی هستند و همچنین در معرض خطر بیشتری برای ابتلا به بیماری های غیرواگیر در بزرگسالی قرار دارند.
اثرات اقتصادی ناشی از اپیدمی چاقی نیز مهم است. اگر کاری انجام نشود، پیش بینی می شود که هزینه های جهانی اضافه وزن و چاقی تا سال 2030 به 3 تریلیون دلار در سال و تا سال 2060 به بیش از 18 تریلیون دلار برسد.
در نهایت، افزایش نرخ چاقی در کشورهای با درآمد کم و متوسط، از جمله در میان گروههای اجتماعی-اقتصادی پایین، به سرعت در حال جهانی شدن مشکلی است که زمانی فقط با کشورهای با درآمد بالا مرتبط بود.
مواجهه با بار مضاعف سوء تغذیه
بسیاری از کشورهای با درآمد کم و متوسط با به اصطلاح بار مضاعف سوء تغذیه روبرو هستند. در حالی که این کشورها همچنان با مشکلات بیماریهای عفونی و سوء تغذیه دست و پنجه نرم میکنند، افزایش سریع عوامل خطر بیماریهای غیرواگیر مانند چاقی و اضافه وزن را نیز تجربه میکنند.
کودکان در کشورهای کم درآمد و متوسط نسبت به تغذیه ناکافی قبل از زایمان، نوزادان و کودکان خردسال آسیب پذیرتر هستند. در عین حال، این کودکان در معرض غذاهای پرچرب، قندی، نمکی، پرانرژی و فقیر از ریزمغذیها قرار میگیرند که از نظر هزینه کمتر و همچنین کیفیت مواد مغذی پایینتری دارند. این الگوهای غذایی، در ارتباط با سطوح پایینتر فعالیت بدنی، منجر به افزایش شدید چاقی در دوران کودکی میشود در حالی که مسائل مربوط به سوء تغذیه حل نشده باقی میماند.
پیشگیری و مدیریت اضافه وزن و چاقی
اضافه وزن و چاقی و همچنین بیماری های غیرواگیر مرتبط با آنها تا حد زیادی قابل پیشگیری و کنترل هستند.

در سطح فردی
افراد ممکن است بتوانند با اتخاذ مداخلات پیشگیرانه در هر مرحله از چرخه زندگی، از قبل از بارداری و ادامه در سال های اولیه، خطر خود را کاهش دهند. این شامل:
- اطمینان از افزایش وزن مناسب در دوران بارداری؛
- تغذیه انحصاری با شیر مادر در 6 ماه اول پس از تولد و ادامه شیردهی تا 24 ماهگی یا بیشتر.
- حمایت از رفتارهای کودکان در مورد تغذیه سالم، فعالیت بدنی، رفتارهای بی تحرک و خواب، صرف نظر از وضعیت وزن فعلی.
- محدود کردن زمان صفحه نمایش ها؛
- محدود کردن مصرف نوشیدنی های شیرین شده با شکر و غذاهای پرانرژی وترویج سایر رفتارهای غذایی سالم.
- لذت بردن از یک زندگی سالم (رژیم غذایی سالم، فعالیت بدنی، مدت و کیفیت خواب، اجتناب از دخانیات و الکل، خودتنظیمی عاطفی)؛
- محدود کردن دریافت انرژی از کل چربی ها و قندها و افزایش مصرف میوه و سبزیجات و همچنین حبوبات، غلات کامل و آجیل.
- پرداختن به فعالیت بدنی منظم.

پزشکان نیز باید به
- به ارزیابی وزن و قد افرادی که به امکانات بهداشتی دسترسی دارند بپردازند.
- مشاوره در مورد رژیم غذایی سالم و سبک زندگی ارائه دهند؛
- هنگامی که تشخیص چاقی مشخص شد، خدمات بهداشتی یکپارچه پیشگیری و مدیریت چاقی از جمله رژیم غذایی سالم، فعالیت بدنی و اقدامات پزشکی و جراحی را ارائه دهند. و
- سایر عوامل خطر بیماری غیرواگیر (گلوکز خون، لیپیدها و فشار خون) را پایش کرده و وجود بیماریهای همراه و ناتوانی از جمله اختلالات سلامت روان را ارزیابی کنند.
شرایط محیطی و اجتماعی
الگوهای رژیم غذایی و فعالیت بدنی برای افراد تا حد زیادی نتیجه شرایط محیطی و اجتماعی است که انتخاب شخصی را به شدت محدود می کند. چاقی یک مسئولیت اجتماعی و نه فردی است و راهحلهایی را میتوان از طریق ایجاد محیطها و جوامع حمایتی که رژیمهای غذایی سالم و فعالیت بدنی منظم را بهعنوان در دسترسترین و مقرون به صرفهترین رفتارهای زندگی روزمره قرار میدهند، یافت.
توقف افزایش چاقی مستلزم اقدامات چند بخشی مانند تولید مواد غذایی، بازاریابی و قیمت گذاری و موارد دیگر است که به دنبال رسیدگی به عوامل تعیین کننده گسترده تر سلامت (مانند کاهش فقر و برنامه ریزی شهری) هستند.
این گونه سیاست ها و اقدامات عبارتند از:
- اقدامات ساختاری، مالی و نظارتی با هدف ایجاد محیط های غذایی سالم که گزینه های غذایی سالم تر را در دسترس، در دسترس و مطلوب قرار دهد. و
- پاسخهای بخش سلامت برای شناسایی خطر، پیشگیری، درمان و مدیریت بیماری طراحی و تجهیز شده است. این اقدامات باید بر اساس تلاشهای گستردهتر برای مقابله با بیماریهای غیرواگیر و تقویت سیستمهای بهداشتی از طریق رویکرد مراقبتهای بهداشتی اولیه انجام شوند و در آنها ادغام شوند.

صنایع غذایی می تواند نقش مهمی در ترویج رژیم غذایی سالم داشته باشد که از طریق:
- کاهش چربی، قند و نمک غذاهای فرآوری شده؛
- اطمینان از اینکه انتخاب های سالم و مغذی در دسترس و مقرون به صرفه برای همه مصرف کنندگان است.
- محدود کردن بازاریابی غذاهای سرشار از قند، نمک و چربی، به ویژه غذاهایی که برای کودکان و نوجوانان هدف قرار می گیرند. و
- اطمینان از در دسترس بودن انتخاب های غذایی سالم و حمایت از تمرین منظم فعالیت بدنی در محل کار.
منبع مطالب:
https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight
منبع تصاویر :
https://www.who.int/news-room/facts-in-pictures/detail/6-facts-on-obesity
https://iris.who.int/bitstream/handle/10665/43601/9789241595070_E_eng.pdf?sequence=5&isAllowed=y
مقاومت ضد میکروبی و وضعیت کنونی از نظر سازمان جهانی بهداشت
هفته جهانی آگاهی AMR: پیشگیری از مقاومت ضد میکروبی با هم
هفته جهانی آگاهی از مقاومت ضد میکروبی ( AMR ) که از 18 تا 24 نوامبر (27 آبان تا 3 آذر) می باشد، سازمان جهانی بهداشت (WHO) بر اقدامات فوری مورد نیاز برای توقف مقاومت ضد میکروبی تمرکز دارد.
مقاومت ضد میکروبی یا Antimicrobial resistance (AMR یا AR)
AMR زمانی اتفاق میافتد که باکتریها، ویروسها، قارچها و انگلها دیگر به مواد فعال یا عوامل ضد میکروبی در داروهایی که برای درمان آنها استفاده میشوند پاسخ نمیدهند. هنگامی که آنتی بیوتیک ها (که برای درمان عفونت های باکتریایی استفاده می شوند) و سایر عوامل ضد میکروبی بی اثر می شوند، درمان عفونت ها دشوار یا غیرممکن می شود و خطر گسترش بیماری، بیماری شدید و مرگ را افزایش می دهد.
AMR تنها سالانه باعث مرگ 5 میلیون انسان در اثر عفونت های باکتریایی می شود. این امر، همراه با وضعیت ضعیف سرمایهگذاری تحقیق و توسعه بر روی ضد میکروبیهای جدید، باعث شده است که WHO ، مقاومت ضد میکروبی (AMR) را به عنوان یکی از 10 تهدید برتر بهداشت عمومی جهانی که بشریت با آن مواجه است برجسته کند.
حقایق کلیدی AMR توسط WHO
- مقاومت ضد میکروبی (AMR) یک تهدید جهانی برای سلامت و توسعه است. برای دستیابی به اهداف توسعه پایدار (SDGs) نیاز به اقدام فوری چند بخشی دارد.
- WHO اعلام کرده است که AMR یکی از 10 تهدید بزرگ بهداشت عمومی جهانی است که بشریت با آن مواجه است.
- استفاده نادرست و استفاده بیش از حد از داروهای ضد میکروبی، محرک های اصلی در توسعه پاتوژن های مقاوم به دارو هستند.
- فقدان آب تمیز و بهداشتی و پیشگیری و کنترل ناکافی عفونت باعث گسترش میکروبها میشود که برخی از آنها میتوانند به درمان ضد میکروبی مقاوم باشند.
- هزینه AMR برای اقتصاد قابل توجه است. علاوه بر مرگ و ناتوانی، بیماری طولانی مدت منجر به اقامت طولانیتر در بیمارستان، نیاز به داروهای گرانتر و چالشهای مالی برای افراد آسیبدیده میشود.
- بدون ضد میکروبیهای مؤثر، موفقیت پزشکی مدرن در درمان عفونتها، از جمله در طی جراحیهای بزرگ و شیمیدرمانی سرطان، در خطر بوده و افزایش مییابد.
ضد میکروبی ها چی هستند؟
ضد میکروبی ها - از جمله آنتی بیوتیک ها، ضد ویروس ها، ضد قارچ ها و ضد انگلی ها - داروهایی هستند که برای پیشگیری و درمان عفونت ها در انسان، حیوانات و گیاهان استفاده می شوند.
مقاومت ضد میکروبی چی هست ؟
مقاومت ضد میکروبی (AMR) زمانی اتفاق میافتد که باکتریها، ویروسها، قارچها و انگلها در طول زمان تغییر میکنند و دیگر به داروها پاسخ نمیدهند و درمان عفونتها را سختتر میکنند و خطر گسترش بیماری، بیماری شدید و مرگ را افزایش میدهند. در اثر مقاومت دارویی، آنتی بیوتیک ها و سایر داروهای ضد میکروبی بی اثر می شوند و درمان عفونت ها به طور فزاینده ای دشوار یا غیرممکن می شود.
چرا مقاومت ضد میکروبی یک نگرانی جهانی است؟
ظهور و گسترش پاتوژن های مقاوم به دارو که مکانیسم های مقاومت جدیدی را به دست آورده اند و منجر به مقاومت ضد میکروبی شده است، همچنان توانایی ما را برای درمان عفونت های رایج تهدید می کند. به خصوص گسترش هشدار دهنده سریع جهانی، باکتری های مقاوم multi and pan-resistant bacteria که به عنوان "superbugs" نیز شناخته می شوند، که باعث عفونت هایی می شود که با داروهای ضد میکروبی موجود مانند آنتی بیوتیک ها قابل درمان نیستند.
آنتیبیوتیکها بهطور فزایندهای بیاثر میشوند، زیرا مقاومت دارویی در سطح جهان گسترش مییابد که منجر به دشوارتر شدن درمان عفونتها و مرگ میشود. آنتی باکتریال های جدید به فوریت مورد نیاز است - برای مثال، برای درمان عفونت های باکتریایی گرم منفی مقاوم به کارباپنم، همانطور که در لیست پاتوژن اولویت سازمان جهانی بهداشت شناسایی شده است. با این حال، اگر مردم در حال حاضر روش مصرف آنتی بیوتیک ها را تغییر ندهند [منظور مصرف خودسرانه و بدون تجویز دکتر]، این آنتی بیوتیک های جدید به سرنوشت آنتی بیوتیک های فعلی دچار می شوند و بی اثر می شوند.
چه چیزی ظهور و گسترش مقاومت ضد میکروبی را تسریع می کند؟
AMR به طور طبیعی در طول زمان و معمولاً از طریق تغییرات ژنتیکی رخ می دهد. ارگانیسم های مقاوم به ضد میکروبی در افراد، حیوانات، غذا، گیاهان و محیط زیست (در آب، خاک و هوا) یافت می شوند. آنها می توانند از فردی به فرد دیگر یا بین افراد و حیوانات، از جمله از مواد غذایی با منشاء حیوانی، سرایت کنند. محرک اصلی مقاومت ضد میکروبی شامل استفاده نادرست و استفاده بیش از حد از داروهای ضد میکروبی است. همچنین عدم دسترسی به آب تمیز و بهداشتی هم برای انسان و هم برای حیوانات، و نبود سیستم تخلیه فاضلاب بهداشتی؛ پیشگیری و کنترل ضعیف عفونت و بیماری در مراکز مراقبت بهداشتی و مزارع؛ دسترسی ضعیف به داروهای با کیفیت، واکسنها و دستگاههای تشخیصی؛ عدم آگاهی و دانش؛ و عدم اجرای قانون از دیگر عوامل موثر در گسترش مقاومت ضد میکروبی می باشند.
وضعیت کنونی مقاومت دارویی در باکتری ها، ویروس ها، انگل و قارچ
- مقاومت دارویی در باکتری ها
برای عفونتهای باکتریایی رایج، از جمله عفونتهای دستگاه ادراری، سپسیس، عفونتهای مقاربتی، و برخی از اشکال اسهال، میزان بالایی از مقاومت در برابر آنتیبیوتیکهایی که اغلب برای درمان این عفونتها استفاده میشوند، در سراسر جهان مشاهده شده است که نشان میدهد در آنتیبیوتیکهای مؤثر در حال اتمام هستیم.
به عنوان مثال، میزان مقاومت به سیپروفلوکساسین، آنتی بیوتیکی که معمولاً برای درمان عفونتهای دستگاه ادراری استفاده میشود، از 8.4٪ تا 92.9٪ برای Escherichia coliand از 4.1٪ تا 79.4٪ برای کلبسیلا پنومونیه در کشورهایی که به مقاومت ضد میکروبی و مصرف جهانی گزارش می دهند متفاوت است.
کلبسیلا پنومونیه ( K. pneumoniae) باکتری رایج روده است که می تواند باعث عفونت های تهدید کننده زندگی شود. مقاومت در K. pneumoniae به آخرین راه درمان (آنتی بیوتیک های کارباپنم) در تمام مناطق جهان گسترش یافته است. K. pneumoniae عامل اصلی عفونت های بیمارستانی مانند ذات الریه، عفونت های جریان خون و عفونت در نوزادان و بیماران بخش مراقبت های ویژه است. در برخی کشورها، آنتیبیوتیکهای کارباپنم در بیش از نیمی از بیمارانی که برای عفونتهای K.pneumoniae تحت درمان قرار میگیرند، به دلیل مقاومت مؤثر نیستند.
مقاومت به آنتی بیوتیک های فلوروکینولون در E. coli که برای درمان عفونت های دستگاه ادراری استفاده می شود، گسترده است. در بسیاری از نقاط جهان کشورهایی وجود دارند که این روش درمانی اکنون در بیش از نیمی از بیماران بی اثر است.
کولیستین تنها آخرین راه حل برای عفونت های تهدید کننده حیات ناشی از انتروباکتریاسه های مقاوم به کارباپنم (به عنوان مثال E.coli، کلبسیلا و غیره) است. باکتریهای مقاوم به کولیستین نیز در چندین کشور و منطقه شناسایی شدهاند که باعث عفونتهایی میشوند که در حال حاضر درمان آنتیبیوتیکی مؤثری برای آنها وجود ندارد.
باکتری استافیلوکوکوس اورئوس بخشی از فلور پوست ما است و همچنین یکی از علل شایع عفونت در جامعه و مراکز مراقبت بهداشتی است. احتمال مرگ افراد مبتلا به عفونت استافیلوکوکوس اورئوس مقاوم به متی سیلین (MRSA) 64 درصد بیشتر از افراد مبتلا به عفونت های حساس به دارو است.
مقاومت گسترده در سویه های بسیار متغیر N. gonorrhoeae مدیریت و کنترل سوزاک را به خطر انداخته است. مقاومت به سولفونامیدها، پنی سیلین ها، تتراسایکلین ها، ماکرولیدها، فلوروکینولون ها و سفالوسپورین های نسل اولیه به سرعت پدیدار شده است. در حال حاضر، در بیشتر کشورها، سفتریاکسون سفالوسپورین وسیع الطیف تزریقی (ESC) تنها تک درمانی تجربی باقیمانده برای سوزاک است.
مقاومت دارویی در مایکوباکتریوم توبرکلوزیس
سویه های مایکوباکتریوم توبرکلوزیس مقاوم به آنتی بیوتیک پیشرفت در مهار اپیدمی جهانی سل را تهدید می کند. WHO تخمین میزند که در سال 2018، حدود نیم میلیون مورد جدید سل مقاوم به ریفامپیسین (RR-TB) در سطح جهان شناسایی شده است که اکثریت قریب به اتفاق آنها دارای سل مقاوم به چند دارو (MDR-TB) هستند، نوعی سل که به دو قوی ترین داروی ضد سل مقاوم است. تنها یک سوم از حدود نیم میلیون نفری که در سال 2018 به MDR/RR-TB مبتلا شدند، شناسایی و گزارش شدند. MDR-TB مستلزم دورههای درمانی طولانیتر، کمتر مؤثر و بسیار گرانتر از دورههای درمانی سل غیرمقاوم است. کمتر از 60 درصد از افرادی که برای MDR/RR-TB درمان شدهاند با موفقیت درمان میشوند.
در سال 2018، حدود 3.4 درصد از موارد جدید سل و 18 درصد از مواردی که قبلاً تحت درمان قرار گرفته بودند، دارای MDR-TB/RR-TB ( یعنی سل مقاوم به ریفامپیسین و سل مقاوم به چند دارو) بودند و ظهور مقاومت به داروهای جدید «آخرین راه حل» سل برای درمان سل مقاوم به دارو، یک تهدید بزرگ است.
- مقاومت دارویی در ویروس ها

مقاومت دارویی ضد ویروسی یک نگرانی فزاینده در جمعیت بیماران با نقص ایمنی است، جایی که تکثیر مداوم ویروسی و قرار گرفتن در معرض طولانی مدت دارو منجر به انتخاب سویههای مقاوم میشود. مقاومت به اکثر داروهای ضد ویروسی از جمله داروهای ضد رتروویروسی (ARV) ایجاد شده است. همه داروهای ضد رتروویروسی (ARV)،بخصوص در رده های جدیدتر، به دلیل ظهور HIV (HIVDR) مقاوم به دارو در معرض خطر غیرفعال شدن تا حدی یا کامل هستند.
افزایش سطوح مقاومت پیامدهای اقتصادی مهمی دارد زیرا رژیم های دارویی خط دوم و سوم بسیار گران تر از داروهای خط اول هستند. برنامه مقاومت به داروهای HIV سازمان جهانی بهداشت در حال نظارت بر انتقال و ظهور مقاومت به داروهای قدیمی و جدیدتر HIV در سراسر جهان است.
- مقاومت دارویی در انگل های مالاریا
ظهور انگل های مقاوم به دارو یکی از بزرگترین تهدیدها برای کنترل مالاریا است و منجر به افزایش مرگ و میر مالاریا می شود. درمانهای ترکیبی مبتنی بر آرتمیزینین (ACTs) خط اول درمان توصیهشده برای مالاریا P. falciparum بدون عارضه هستند و در اکثر کشورهای آندمیک (بومی) مالاریا استفاده میشوند. مقاومت جزئی به آرتمیزینین و مقاومت به تعدادی از داروهای شریک ACT در کامبوج، جمهوری دموکراتیک خلق لائوس، میانمار، تایلند و ویتنام از طریق مطالعات تایید شده است. بین سال های 2001 تا 2019 انجام شد. این امر انتخاب درمان مناسب را چالش برانگیزتر می کند و نیاز به نظارت دقیق دارد.
در منطقه مدیترانه شرقی WHO [ایران جزو همین منطقه است]، مقاومت P. falciparum به سولفادوکسین- پیریمتامین منجر به شکست آرتسونات- سولفادوکسین- پیریمتامین در برخی کشورها شد که نیاز به تغییر به ACT دیگری را ایجاب کرد.
در آفریقا، اخیراً شواهدی منتشر شده است که نشان دهنده ظهور جهش های مرتبط با مقاومت جزئی آرتمیزینین در رواندا است. تاکنون، ACT هایی که آزمایش شده اند بسیار کارآمد هستند. با این حال، گسترش بیشتر مقاومت به آرتمیزینین و داروهای شریک ACT می تواند یک چالش بزرگ بهداشت عمومی باشد و دستاوردهای مهم در کنترل مالاریا را به خطر بیندازد.
- مقاومت دارویی در قارچ ها

شیوع عفونتهای قارچی مقاوم به دارو در حال افزایش است و وضعیت درمان دشوار را تشدید میکند. بسیاری از عفونت های قارچی دارای مشکلات قابل درمان از جمله سمیت به ویژه برای بیماران مبتلا به سایر عفونت های زمینه ای (مانند HIV) هستند. کاندیدا اوریس مقاوم به دارو، یکی از شایعترین عفونتهای قارچی مهاجم، در حال حاضر با افزایش مقاومت گزارش شده به فلوکونازول، آمفوتریسین B و وریکونازول و همچنین مقاومت در برابر کاسپوفونژین در حال ظهور گسترده است.
این امر منجر به دشوارتر شدن درمان عفونتهای قارچی، شکستهای درمانی، اقامت طولانیتر در بیمارستان و گزینههای درمانی بسیار گرانتر میشود. WHO در حال بررسی جامع عفونتهای قارچی در سطح جهانی است و فهرستی از پاتوژنهای قارچی با اهمیت بهداشت عمومی را همراه با تجزیه و تحلیل خط لوله توسعه ضد قارچی منتشر خواهد کرد.
منبع مطالب
سایت سازمان جهانی بهداشت
https://www.who.int/news-room/fact-sheets/detail/antimicrobial-resistance
https://www.who.int/news/item/17-11-2023-world-amr-awareness-week--preventing-antimicrobial-resistance-together
هر ساعت بیش از 1000 نفر بر اثر سکته مغزی و حمله قلبی جان خود را از دست می دهند
بیشتر این مرگها ناشی از فشار خون بالا است و میتوان از بسیاری از آنها پیشگیری کرد.

اولین گزارش WHO درجزئیات تأثیر مخرب فشار خون بالا و راه های جلوگیری از آن
19 سپتامبر 2023
سازمان جهانی بهداشت (WHO) اولین گزارش خود را در مورد تأثیر مخرب فشار خون بالا در جهان به همراه توصیه هایی در مورد راه های پیروزی در رقابت با این قاتل خاموش منتشر کرد. این گزارش نشان می دهد که از هر 5 نفر مبتلا به فشار خون، 4 نفر به اندازه کافی درمان نمی شوند، اما اگر کشورها بتوانند پوشش خود را افزایش دهند، می توان از 76 میلیون مرگ بین سال های 2023 تا 2050 جلوگیری کرد.
فشار خون از هر 3 بزرگسال در سراسر جهان 1 نفر را تحت تاثیر قرار می دهد. این بیماری شایع و کشنده منجر به سکته مغزی، حمله قلبی، نارسایی قلبی، آسیب کلیه و بسیاری از مشکلات سلامتی دیگر می شود.
تعداد افراد مبتلا به فشار خون (فشار خون 90/140 میلیمتر جیوه یا بالاتر یا مصرف کنندگان داروهای فشار خون بالا) بین سالهای 1990 تا 2019 دو برابر شد و از 650 میلیون به 1.3 میلیارد نفر رسید. تقریباً نیمی از افراد مبتلا به فشار خون در سراسر جهان در حال حاضر از وضعیت خود بی اطلاع هستند. بیش از سه چهارم بزرگسالان مبتلا به فشار خون بالا در کشورهای کم درآمد و متوسط زندگی می کنند.
سن بالاتر و ژنتیک می تواند خطر ابتلا به فشار خون بالا را افزایش دهد، اما عوامل خطر قابل اصلاح مانند خوردن رژیم غذایی پر نمک، عدم تحرک بدنی و نوشیدن بیش از حد الکل نیز می تواند خطر ابتلا به فشار خون را افزایش دهد.
تغییرات سبک زندگی مانند داشتن یک رژیم غذایی سالم، ترک سیگار و تحرک بیشتر می تواند به کاهش فشار خون کمک کند. برخی از افراد ممکن است به داروهایی نیاز داشته باشند که بتواند فشار خون بالا را به طور موثر کنترل کرده و از عوارض مرتبط جلوگیری کند.
پیشگیری، تشخیص زودهنگام و مدیریت موثر فشار خون بالا از جمله مقرونبهصرفهترین مداخلات در مراقبتهای بهداشتی است و باید توسط کشورها به عنوان بخشی از بسته ملی مزایای سلامت ارائه شده در سطح مراقبتهای اولیه اولویتبندی شود. مزایای اقتصادی برنامه های بهبود یافته درمان فشار خون بیش از هزینه های آن حدود 18 به 1 است.
فشار خون بالا را می توان به طور موثر با رژیم های دارویی ساده و کم هزینه کنترل کرد، اما از هر پنج نفر مبتلا به فشار خون فقط یک نفر آن را کنترل کرده است. دکتر تدروس آدهانوم گبریسوس، مدیر کل WHO گفت. «برنامههای کنترل فشار خون نادیده گرفته شده، اولویتبندی نشده و بودجه بسیار کم است. تقویت کنترل فشار خون باید بخشی از سفر هر کشور به سمت پوشش همگانی سلامت، مبتنی بر سیستمهای بهداشتی با عملکرد خوب، عادلانه و انعطافپذیر باشد که بر پایه مراقبتهای اولیه بهداشتی بنا شده است.»
این گزارش در طول هفتاد و هشتمین نشست مجمع عمومی سازمان ملل متحد ارائه می شود که به پیشرفت اهداف توسعه پایدار از جمله اهداف بهداشتی در زمینه آمادگی و واکنش به بیماری همه گیر، پایان دادن به سل و دستیابی به پوشش همگانی سلامت می پردازد. پیشگیری و کنترل بهتر فشار خون بالا برای پیشرفت در همه این موارد ضروری است.
افزایش تعداد بیمارانی که به طور موثر برای فشار خون بالا درمان می شوند تا سطوح مشاهده شده در کشورهای با عملکرد بالا می تواند از 76 میلیون مرگ، 120 میلیون سکته، 79 میلیون حمله قلبی و 17 میلیون مورد نارسایی قلبی از هم اکنون تا سال 2050 جلوگیری کند.
مایکل آر. بلومبرگ، سفیر جهانی بیماریهای غیرواگیر و آسیبهای سازمان جهانی بهداشت، گفت: «اکثر حملات قلبی و سکته مغزی در جهان امروز با داروهای مقرونبهصرفه، ایمن، در دسترس و سایر مداخلات مانند کاهش سدیم قابل پیشگیری هستند. "درمان فشار خون بالا از طریق مراقبت های بهداشتی اولیه جان انسان ها را نجات می دهد، در حالی که میلیاردها دلار در سال صرفه جویی می کند."
فشار خون را می توان به راحتی با داروهای عمومی ایمن، در دسترس و کم هزینه با استفاده از برنامه هایی مانند HEARTS درمان کرد. بسته فنی WHO HEARTS برای مدیریت بیماری های قلبی عروقی در مراقبت های بهداشتی اولیه و راهنمای درمان دارویی فشار خون در بزرگسالان گام های اثبات شده و عملی را برای ارائه مراقبت های موثر فشار خون در محیط های مراقبت های بهداشتی اولیه ارائه می دهد.
مدیریت موثر فشار خون در سطح جامعه و کشور را می توان در کشورهایی با هر سطح درآمدی به دست آورد. بیش از 40 کشور با درآمد کم و متوسط، از جمله بنگلادش، کوبا، هند و سریلانکا، مراقبت های فشار خون خود را با بسته HEARTS تقویت کرده اند و بیش از 17 میلیون نفر را در برنامه های درمانی ثبت نام کرده اند. کشورهایی مانند کانادا و کره جنوبی برنامه های ملی جامع درمان فشار خون را ارائه کردند و هر دو کشور از مرز 50 درصد برای کنترل فشار خون در بزرگسالان مبتلا به فشار خون بالا فراتر رفتند. برنامههای پایدار و سیستماتیک ملی کنترل فشار خون میتوانند موفق شوند و سطح بالای کنترل فشار خون منجر به سکتههای مغزی و حملات قلبی کمتر و زندگی طولانیتر و سالمتر میشود.
این گزارش بر اهمیت اجرای مراقبت های موثر فشار خون توصیه شده توسط WHO برای نجات جان افراد تاکید می کند که شامل پنج جزء زیر است:
- پروتکل: پروتکلهای درمانی عملی دوز و دارو با مراحل عملی خاص برای مدیریت فشار خون کنترلنشده میتواند مراقبت را سادهتر کرده و پایبندی را بهبود بخشد.
- تامین دارو و تجهیزات: دسترسی منظم و بدون وقفه به داروهای مقرون به صرفه برای درمان موثر فشار خون ضروری است. در حال حاضر، قیمت داروهای ضروری ضد فشار خون بین کشورها بیش از ده برابر متفاوت است.
- مراقبت مبتنی بر تیم: زمانی که یک تیم برای تنظیم و تشدید رژیمهای دارویی فشار خون بر اساس دستورات و پروتکلهای پزشک همکاری میکند، نتایج بیمار بهبود مییابد.
- خدمات بیمار محور: برای کاهش موانع مراقبت از طریق ارائه رژیم های دارویی آسان، داروهای رایگان و ویزیت های پیگیری نزدیک به خانه، و در دسترس قرار دادن نظارت بر فشار خون.
- سیستمهای اطلاعاتی: سیستمهای اطلاعاتی ساده و متمرکز بر کاربر، ثبت سریع دادههای ضروری در سطح بیمار را تسهیل میکنند، بار ورود دادههای کارکنان مراقبتهای بهداشتی را کاهش میدهند و همزمان با حفظ یا بهبود کیفیت مراقبت، از افزایش سریع مقیاس پشتیبانی میکنند.
هر ساعت بیش از 1000 نفر بر اثر سکته مغزی و حمله قلبی جان خود را از دست می دهند. دکتر تام فریدن، رئیس و مدیر عامل شرکت Resolve to Save Lives، گفت: بیشتر این مرگها ناشی از فشار خون بالا است و میتوان از بسیاری از آنها پیشگیری کرد. "مراقبت خوب فشار خون بالا مقرون به صرفه است، در دسترس است و مراقبت های بهداشتی اولیه را تقویت می کند. چالش در حال حاضر این است که از "در دسترس" به " دسترسی داشتن" بروید. این مستلزم تعهد دولتهای سراسر جهان است.»
منبع مطالب و تصاویر سایت سازمان جهانی بهداشت و در اینجا می توانید ببینید.
https://www.who.int/news/item/19-09-2023-first-who-report-details-devastating-impact-of-hypertension-and-ways-to-stop-it
https://www.who.int/news-room/fact-sheets/detail/hypertension
https://www.who.int/news/item/25-08-2021-more-than-700-million-people-with-untreated-hypertension
آپلود عکس های این مطلب از اینجا بود.
آبله میمونی و اقدامات محافظتی
مقدمه
آبله میمونی یک بیماری عفونی قابل انتقال از حیوان به انسان است که توسط ویروس آبله میمونی ایجاد میشود. این بیماری میتواند از فردی به فرد دیگر منتقل شود.
علائم
آبله میمونی معمولا شامل
- تب
- سردرد شدید
- دردهای عضلانی
- کمردرد
- ضعف
- تورم غدد لنفاوی
- بثورات یا تاولهای پوستی
بثورات یا تاولهای پوستی معمولا در عرض یک تا سه روز پس از شروع تب آشکار میشود. تاولها ممکن است صاف یا کمی برجسته باشند، با مایع شفاف یا زرد پر شده و سپس پوسته پوسته و خشک شوند و بریزند.
تعداد تاولها در یک فرد میتواند از چند عدد تا چند هزار تاول متغیر باشد. بثورات روی صورت، کف دستها و کف پا متمرکز میشوند. این بثورات میتوانند در دهان، اندام تناسلی و چشم یافت شوند. نوزادان، کودکان و افراد مبتلا به نقص ایمنی زمینه ای ممکن است در معرض خطر علائم جدی تر و مرگ ناشی از آبله میمونی باشند.
انتقال
افراد آلوده به ویروس آبله میمونی از زمان بروز علائم تا خاتمه آن (به طور معمول بین دو تا چهار هفته) عفونی هستند( یعنی قدرت انتقال بیماری به اطرافیان را دارند). ابتلا به آبله میمونی از طریق
- تماس فیزیکی نزدیک با فردی که علائم دارد، میتواند اتفاق بیفتد. بثورات پوستی، مایعات بدن (مانند آب، چرک یا خون ناشی از ضایعات پوستی) و دلمه ها به ویژه عفونی هستند.
- لباس، ملحفه، حوله یا اشیایی مانند قاشق و چنگال/ ظروف غذاخوری که در اثر تماس با فرد مبتلا به ویروس آلوده شده اند نیز میتوانند دیگران را مبتلا نمایند.
- زخمها، ضایعات یا زخمهای دهان نیز میتوانند عفونی باشند، به این معنی که ویروس میتواند از طریق بزاق انتشار یابد.
- از طریق جفت از مادر به جنین یا از طریق تماس پوست به پوست از والدین به کودکان منتقل شود. این ویروس همچنین میتواند از طریق تماس فیزیکی اولیه از مادر به نوزاد منتقل گردد.
بنابراین افرادی که از نزدیک با فردی که مبتلا به بیماری در ارتباط میباشند، از جمله کارکنان بهداشتی و اعضای خانواده در معرض خطر بیشتری برای عفونت هستند.
افراد در معرض خطر
- نوزادان، کودکان و افراد مبتلا به نقص ایمنی
- تماس فیزیکی با حیوان آلوده یا فرد مبتلا به آبله میمونی
- کارکنان بهداشتی نیز به دلیل قرار گرفتن طوالنیتر در معرض ویروس
کودکان معمولابیشتر از نوجوانان و بزرگسالان مستعدابتلا به علائم شدید آبله میمونی هستند.
اقدامات احتیاطی
برای ارائه دهندگان مراقبتهای بهداشتی و درمانی شامل :
- ایزوله نمودن شخص آلوده
- در صورت امکان پوشاندن ضایعات پوستی
- حداقل رساندن تماس فیزیکی با فرد بیمار یا مشکوک به بیماری
- الزام استفاده از ماسک (به خصوص اگر بیمار سرفه میکند و یا ضایعات دهانی دارد) برای بیمار، کارکنان ارائه کننده خدمات تشخیصی، بهداشتی درمانی، افراد خانواده و همراه بیمار
- الزام استفاده از ماسک و دستکش یکبار مصرف هنگام تماس مستقیم با ضایعات
- الزام استفاده از ماسک و دستکش یکبار مصرف هنگام دست زدن به لباس یا ملحفه بیمار
منبع : راهنمای الزامات سلامت محیط و کاردر مقابله با بیماری بیماری آبله میمونی - دفتر آموزش و ارتقاء سلامت
https://iec.behdasht.gov.ir/uploads/143/2022/Aug/17/%D8%A7%D9%84%D8%B2%D8%A7%D9%85%D8%A7%D8%AA_1.pdf
آبله میمونی
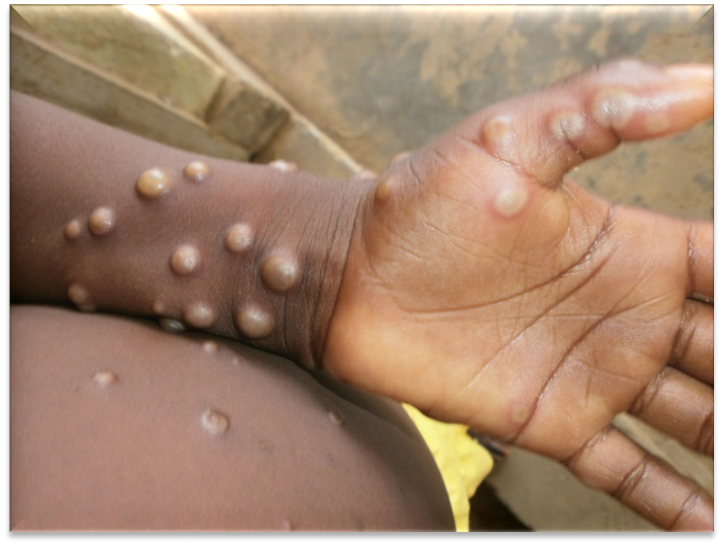
حقایق کلیدی آبله میمونی از سوی سازمان بهداشت جهانی (WHO)
- واکسن های مورد استفاده در برنامه ریشه کنی آبله نیز محافظت در برابر آبله میمون را فراهم کردند.
- واکسنهای جدیدتری ساخته شدهاند که یکی از آنها برای پیشگیری از آبله میمون تایید شده است.
- آبله میمون معمولاً یک بیماری خود محدود شونده است که علائم آن بین 2 تا 4 هفته طول می کشد.
- موارد شدید ممکن است رخ دهد. در زمان های اخیر، نسبت مرگ و میر در حدود 3-6٪ بوده است .
- آبله میمون از طریق تماس نزدیک با شخص یا حیوان آلوده یا مواد آلوده به ویروس، به انسان منتقل می شود.
- ویروس آبله میمون از طریق تماس نزدیک با ضایعات، مایعات بدن، قطرات تنفسی و مواد آلوده مانند ملافه و لوازم تخت خواب از فردی به فرد دیگر منتقل می شود.
- آبله میمون یک بیماری مشترک بین انسان و دام است که عمدتاً در مناطق جنگل های بارانی استوایی مرکز و غرب آفریقا رخ می دهد و گهگاه به مناطق دیگر صادر می شود.
- یک عامل ضد ویروسی توسعه یافته برای درمان آبله نیز برای درمان آبله میمون مجوز گرفته است.
- تظاهرات بالینی آبله میمون شبیه آبله است، یک عفونت ارتوپاکس ویروس مرتبط که در سال 1980 در سراسر جهان ریشه کن شده اعلام شد.
- آبله میمون کمتر از آبله مسری است و باعث بیماری کمتری می شود.
- آبله میمون معمولاً از نظر بالینی با تب، بثورات و غدد لنفاوی متورم تظاهر میکند و ممکن است منجر به طیف وسیعی از عوارض پزشکی شود.
ادامه مطلب اینجا کلیک شود.
مرور کلی بیماری
ویروس آبله میمون یک ویروس ارتوپاکس است که باعث ایجاد بیماری با علائمی مشابه آبله اما با شدت کمتر می شود. در حالی که آبله در سال 1980 ریشه کن شد، آبله میمون همچنان در کشورهای مرکز و غرب آفریقا رخ می دهد.
آبله میمون یک بیماری مشترک انسان و دام است: بیماری که از حیوانات به انسان منتقل می شود. موارد اغلب در نزدیکی جنگل های بارانی استوایی یافت می شود که در آن حیوانات حامل ویروس وجود دارند. شواهدی از عفونت ویروس آبله میمون در حیواناتی از جمله سنجاب، موش صحرایی گامبیایی، موش زمستان خواب، گونه های مختلف میمون و غیره یافت شده است.
انتقال از انسان به انسان محدود است و طولانی ترین زنجیره انتقال مستند 6 نسل است، به این معنی که آخرین فردی که در این زنجیره آلوده شده است 6 حلقه از فرد بیمار اصلی فاصله داشته است. از طریق تماس با مایعات بدن، ضایعات روی پوست یا سطوح مخاطی داخلی مانند دهان یا گلو، قطرات تنفسی و اشیاء آلوده قابل انتقال است.
تشخیص DNA ویروسی با واکنش زنجیره ای پلیمراز (PCR) بهترین آزمایش آزمایشگاهی برای آبله میمون است. بهترین نمونه های تشخیصی مستقیماً از بثورات پوستی، مایع یا پوسته، یا بیوپسی در صورت امکان می باشد.
علایم بیماری
آبله میمون با تب و راش (بثورات پوستی) مشخص گسترده و معمولاً غدد لنفاوی متورم تظاهر میکند. تشخیص آبله میمون از سایر بیماری ها مانند آبله مرغان، سرخک، عفونت های باکتریایی پوست، گال، سیفلیس و آلرژی های مرتبط با دارو بسیار مهم است.
دوره کمون آبله میمون می تواند از 5 تا 21 روز متغیر باشد. مرحله تب دار بیماری معمولاً 1 تا 3 روز با علائمی مانند تب، سردرد شدید، لنفادنوپاتی (ورم غدد لنفاوی)، کمردرد، میالژی (درد عضلانی) و آستنی شدید (کمبود انرژی) طول میکشد. بعد از مرحله تب دار، مرحله ظهور بثورات پوستی که 2 تا 4 هفته طول می کشد. ضایعات از ماکول (ضایعات با پایه صاف) به پاپول (ضایعات دردناک برجسته) تا وزیکول (ضایعات پر از مایع شفاف) به پوسچول (ضایعات پر از چرک) و به دنبال آن دلمه یا پوسته تکامل مییابند.
نسبت بیمارانی که می میرند در موارد ثبت شده بین 0 تا 11 درصد متغیر بوده و در میان کودکان خردسال بیشتر بوده است.
درمان
درمان بیماران آبله میمونی بسته به علائم به صورت حمایتی است. ترکیبات مختلفی که ممکن است در برابر عفونت ویروس آبله میمون موثر باشند در حال توسعه و آزمایش هستند. پیشگیری و کنترل آبله میمون انسانی متکی بر افزایش آگاهی در جوامع و آموزش کارکنان بهداشتی برای جلوگیری از عفونت و توقف انتقال است.
بیشتر عفونتهای آبله میمون در انسان ناشی از انتقال اولیه از حیوان به انسان است. از تماس با حیوانات بیمار یا مرده باید اجتناب شود و تمام غذاهای حاوی گوشت حیوانی یا قطعات آن باید قبل از مصرف به درستی پخته شوند.
از تماس نزدیک با افراد آلوده یا مواد آلوده باید اجتناب شود. هنگام مراقبت از بیمار، چه در یک مرکز بهداشتی و چه در خانه، باید از دستکش و سایر لباس ها و تجهیزات محافظ شخصی استفاده کرد.
واکسیناسیون علیه آبله در گذشته 85 درصد در پیشگیری از آبله میمون موثر بوده است. اعضای خانواده و جامعه، کارکنان بهداشتی و پرسنل آزمایشگاهی که در دوران کودکی علیه آبله واکسینه شدهاند، ممکن است مقداری محافظت در برابر آبله میمون داشته باشند.
ادامه مطلب اینجا کلیک شود.
همه گیری
آبله میمون انسان برای اولین بار در سال 1970 در جمهوری دموکراتیک کنگو در یک پسر 9 ماهه در منطقه ای که آبله در سال 1968 از بین رفته بود در انسان شناسایی شد. از آن زمان، بیشتر موارد از مناطق روستایی و جنگلی گزارش شده است. حوضه کنگو، به ویژه در جمهوری دموکراتیک کنگو و موارد انسانی به طور فزاینده ای از سراسر آفریقای مرکزی و غربی گزارش شده است.
از سال 1970، موارد انسانی آبله میمون در 11 کشور آفریقایی گزارش شده است: بنین، کامرون، جمهوری آفریقای مرکزی، جمهوری دموکراتیک کنگو، گابن، ساحل عاج، لیبریا، نیجریه، جمهوری کنگو، سیرالئون. و سودان جنوبی بار واقعی آبله میمون مشخص نیست. به عنوان مثال، در سال 1996-1997، شیوع بیماری در جمهوری دموکراتیک کنگو با نسبت مرگ و میر کمتر و نرخ حمله بالاتر از حد معمول گزارش شد.
آبله میمون یک بیماری با اهمیت بهداشت عمومی جهانی است، زیرا نه تنها کشورهای غرب و مرکز آفریقا، بلکه سایر نقاط جهان را نیز درگیر می کند. در سال 2003، اولین شیوع آبله میمون در خارج از آفریقا در ایالات متحده آمریکا بود و با تماس با سگهای خانگی آلوده دشتزار مرتبط بود. این حیوانات خانگی با موشهای کیسهدار گامبیایی و خوابگاهی که از غنا به کشور وارد شده بودند، نگهداری میشدند. این شیوع منجر به بیش از 70 مورد آبله میمون در ایالات متحده شد. آبله میمون نیز در مسافرانی از نیجریه به اسرائیل در سپتامبر 2018، به بریتانیا در سپتامبر 2018، دسامبر 2019، می 2021 و می 2022، به سنگاپور در می 2019 گزارش شده است. و به ایالات متحده آمریکا در ژوئیه و نوامبر 2021. در می 2022، موارد متعدد آبله میمون در چندین کشور غیر بومی شناسایی شد. در حال حاضر مطالعاتی برای درک بیشتر اپیدمیولوژی، منابع عفونت و الگوهای انتقال در حال انجام است.
پیشگیری
افزایش آگاهی از عوامل خطر و آموزش مردم در مورد اقداماتی که می توانند برای کاهش قرار گرفتن در معرض ویروس انجام دهند، استراتژی اصلی پیشگیری از آبله میمون است.
- کاهش خطر انتقال انسان به انسان
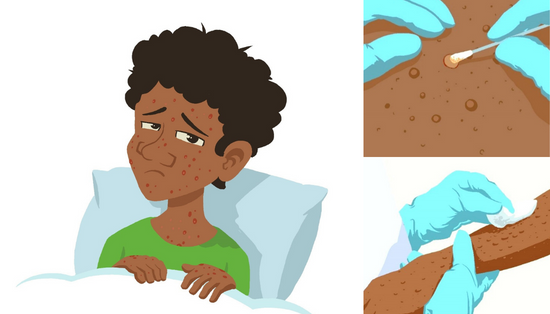
نظارت و شناسایی سریع موارد جدید برای مهار شیوع بسیار مهم است. در طول شیوع آبله میمون انسان، تماس نزدیک با افراد آلوده مهم ترین عامل خطر برای عفونت ویروس آبله میمون است. کارکنان بهداشتی و اعضای خانواده در معرض خطر بیشتری برای ابتلا هستند. کارکنان بهداشتی که از بیماران مبتلا به عفونت مشکوک یا تایید شده ویروس آبله میمون مراقبت می کنند، یا نمونه هایی از آنها را به کار می گیرند، باید اقدامات احتیاطی استاندارد کنترل عفونت را اجرا کنند. در صورت امکان، افرادی که قبلاً علیه آبله واکسینه شده اند باید برای مراقبت از بیمار انتخاب شوند.
نمونه های گرفته شده از افراد و حیوانات مشکوک به عفونت ویروس آبله میمون باید توسط کارکنان آموزش دیده ای که در آزمایشگاه های مجهز کار می کنند، نگهداری شود. نمونه های بیمار باید طبق دستورالعمل سازمان بهداشت جهانی برای حمل و نقل مواد عفونی برای حمل و نقل با بسته بندی سه گانه آماده شوند.
شناسایی خوشههایی از موارد آبله میمون در چندین کشور غیر بومی بدون پیوند مستقیم سفر به یک منطقه بومی در می 2022 غیر معمول است. تحقیقات بیشتر برای تعیین منبع احتمالی عفونت و محدود کردن گسترش بیشتر در حال انجام است. از آنجایی که منبع شیوع این بیماری در حال بررسی است، بررسی همه روش های احتمالی انتقال به منظور حفظ سلامت عمومی مهم است.
- کاهش خطر انتقال انسان و دام
با گذشت زمان، بیشتر عفونت های انسانی ناشی از انتقال اولیه از حیوان به انسان است. از تماس محافظت نشده با حیوانات وحشی، به ویژه حیواناتی که بیمار یا مرده هستند، از جمله گوشت، خون و سایر قسمت های آنها باید اجتناب شود. علاوه بر این، تمام غذاهای حاوی گوشت حیوانی یا قطعات آن باید قبل از مصرف کاملا پخته شوند.
- پیشگیری از آبله میمون از طریق محدودیت در تجارت حیوانات
برخی از کشورها مقرراتی را وضع کرده اند که واردات جوندگان و نخستی های غیر انسانی را محدود می کند. حیوانات اسیر که به طور بالقوه آلوده به آبله میمون هستند باید از سایر حیوانات جدا شده و بلافاصله در قرنطینه قرار داده شوند. هر حیوانی که ممکن است با حیوان آلوده تماس داشته باشد باید قرنطینه شود، با اقدامات احتیاطی استاندارد رفتار شود و علائم آبله میمون به مدت 30 روز تحت نظر باشد.
- ارتباط آبله میمون با آبله
تظاهرات بالینی آبله میمون شبیه آبله است، یک عفونت ارتوپاکس ویروس مرتبط که ریشه کن شده است. آبله راحتتر منتقل میشد و اغلب کشنده بود زیرا حدود 30 درصد از بیماران جان خود را از دست دادند. آخرین مورد آبله به طور طبیعی در سال 1977 رخ داد و در سال 1980 اعلام شد که آبله در سراسر جهان پس از یک کمپین جهانی واکسیناسیون و مهار ریشه کن شده است. 40 سال یا بیشتر از زمانی که همه کشورها واکسیناسیون معمول آبله را با واکسن های مبتنی بر واکسینیا متوقف کرده اند می گذرد. از آنجایی که واکسیناسیون در غرب و مرکز آفریقا در برابر آبله میمون نیز محافظت می کند، جمعیت های واکسینه نشده نیز در حال حاضر بیشتر مستعد ابتلا به عفونت ویروس آبله میمون هستند.
منبع مطالب و تصاویر سایت سازمان جهانی بهداشت
https://www.who.int/news-room/fact-sheets/detail/monkeypox
https://www.who.int/health-topics/monkeypox#tab=tab_3
https://openwho.org/courses/monkeypox-introduction






